在我们日常生活中,分解反应是经常发生的一种化学反应。但是,分解反应是放热还是吸热呢?下面让我们一起来探讨一下这个问题。
1. 我们来了解一下分解反应的定义。分解反应是一种将一个化合物分解成两个或更多简单物质的反应。这种反应通常需要一定的能量来打破化合物中的化学键。
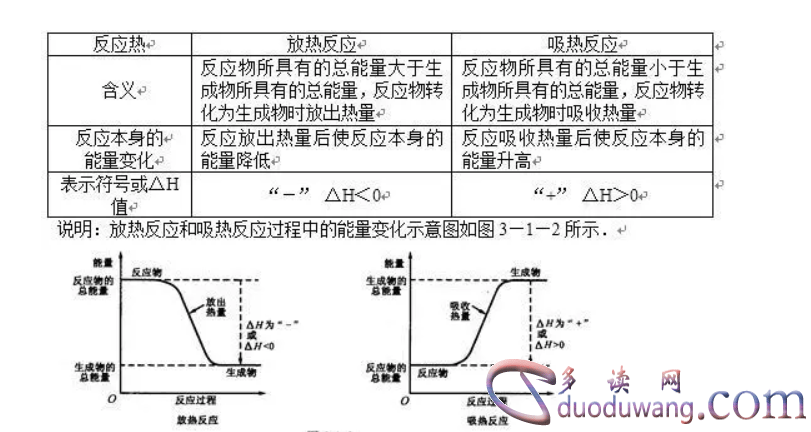
2. 如果在分解反应过程中释放出能量,那么这个反应就是放热反应。这是因为能量被释放出来,使得周围的环境温度升高。
3. 相反,如果在分解反应过程中吸收了能量,那么这个反应就是吸热反应。在吸热反应中,化合物分解所需的能量来自于其周围的环境,使得环境的温度降低。
4. 一个常见的放热反应是氮气和氢气在高温条件下反应生成氨气的反应:
N2(g) + 3H2(g) → 2NH3(g) ΔH = -92.2 kJ/mol
在这个反应中,化学键被打破,导致了能量的释放,使得这个反应是放热反应。
5. 相反,一个常见的吸热反应是碳酸氢钠在加热的条件下分解成碳酸钠、水和二氧化碳:

2NaHCO3(s) → Na2CO3(s) + H2O(g) + CO2(g) ΔH = +128 kJ
在这个反应中,化学键的断裂需要吸收能量,因此这个反应是吸热反应。
6. 另外,分解反应是放热还是吸热还与反应物和生成物之间的键能有关。如果生成物之间的化学键比反应物之间的化学键更强,那么这个反应通常是放热的。反之,如果生成物之间的化学键比反应物之间的化学键更弱,那么这个反应通常是吸热的。
7. 除了温度对反应性质的影响外,催化剂也可以改变一个分解反应是放热还是吸热。催化剂可以降低反应物之间的化学键的断裂能量,从而降低反应的放热性质。因此,在有催化剂存在的情况下,原本是放热反应的分解反应可能变为吸热反应。
8. 总结:分解反应是放热还是吸热取决于反应中的化学键断裂和生成的能量变化。在我们的日常生活中,我们可以通过实验来确定一个分解反应是放热还是吸热,这有助于我们更好地理解化学反应过程。
在化学反应中,分解反应是一种常见的反应类型。通过了解分解反应是放热还是吸热,我们可以更好地预测反应的性质,并且可以更好地控制反应过程。希望这篇文章能帮助您更好地理解分解反应的放热和吸热性质。